环肽合成是多肽化学的重要分支,其核心在于通过构建环状结构,显著增强多肽的稳定性、生物活性与靶向性,因此被广泛应用于药物研发及生物医学研究领域。凭借独特的结构优势,环肽能有效弥补小分子药物与生物药的短板,已成为当前新药研发的关键突破口。在新药研发中,环肽合成主要通过提供高稳定性、高靶向性、高成药性的候选分子,为抗肿瘤、抗感染、代谢疾病等领域的药物创新提供核心支撑。武汉天德生物可提供全方位一站式环肽服务,服务范围覆盖实验室研究、临床前研究、临床申请至临床研究各阶段,能精准匹配不同需求,为您的环肽药物开发项目全程助力!
二硫键环肽
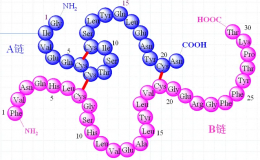
二硫键是众多蛋白质立体结构中不可或缺的组成部分,在几乎所有胞外肽类与蛋白质分子中,都能检测到这类共价键的存在。当一个半胱氨酸的硫原子,与蛋白质中另一位置半胱氨酸的硫原子形成共价单键时,二硫键便随之生成。这类化学键对蛋白质稳定性具有重要作用,尤其能显著增强从细胞中分泌的蛋白质的稳定性。
二硫键的有效形成需涉及多个关键环节,具体包括对半胱氨酸的合理管理、对半胱氨酸残基的保护策略、保护基团的脱除方法,以及半胱氨酸的配对方式等。
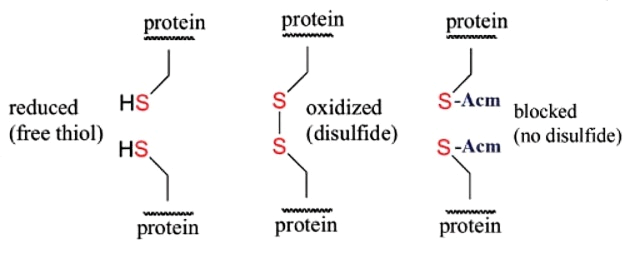
武汉天德生物拥有成熟的二硫键成环技术。当多肽中仅含 1 对 Cys 时,二硫键的形成过程相对简单:先通过固相或液相法完成多肽合成,随后在 pH 8-9 的溶液中进行氧化即可。
若需形成 2 对或 2 对以上的二硫键,合成过程则更为复杂。尽管二硫键的形成通常在合成方案的最后阶段完成,但有时引入预先形成的二硫化物,有助于肽链的连合或延长。武汉天德生物常用的 Cys 保护基团包括 Bzl、Meb、Mob、tBu、Trt、Tmob、TMTr、Acm、Npys 等,且在二硫键多肽合成领域具备显著优势,具体可实现:
- 1. 分子内两对二硫键形成,分子间两对二硫键形成
2. 分子内三对二硫键形成,分子间三对二硫键形成
3. 类胰岛素多肽合成,不同肽序间两对二硫键形成
4. 三对二硫键多肽合成
酰胺键环肽
研究表明,具备 α- 螺旋结构且富含正电荷的多肽能够穿过细胞膜。基于这一特性,人们开发出以二硫键、分子内酰胺键及订书肽为支架的 α- 螺旋结构;其中在酰胺键成环多肽领域,RGD 系列环肽是当前最受关注的研究方向。武汉天德生物可提供多元化酰胺键成环技术服务,具体包括多肽首尾酰胺键成环、多肽侧链酰胺键成环,同时能合成全系列 RGD 环肽。
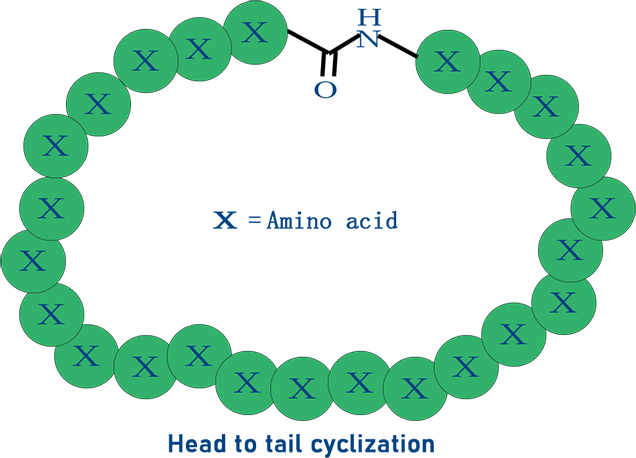
一、酰胺键-多肽首尾成环
武汉天德生物通过对多肽 N 端氨基酸 α- 氨基进行差异化保护与脱除,再将该 α- 氨基与多肽 C 端羧基进行缩合反应,可高效制备高质量首尾环肽,其 HPLC 纯度可达 98%。
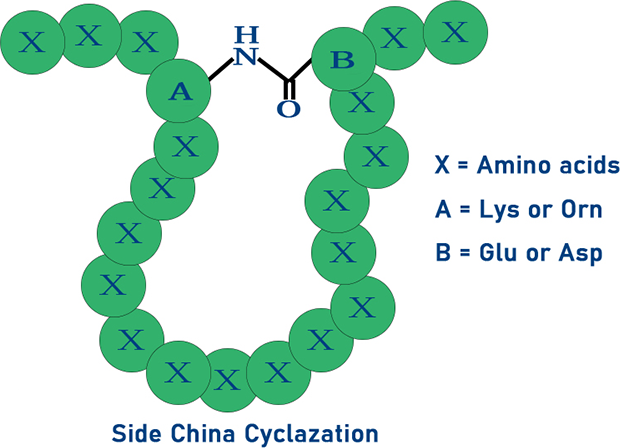
二、酰胺键-多肽侧链成环
武汉天德生物通过对 Lys 或 Orn 的侧链氨基、Glu 或 Asp 的侧链羧基进行选择性保护与脱除,能够实现多肽的精准位点成环,可合成出稳定性强、品质优异的产品。
RGD环肽
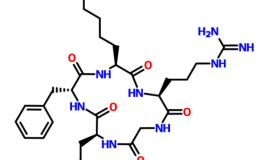
RGD是纤连蛋白中的一类短肽片段,是纤连蛋白与细胞表面受体整合素等物质相互作用的关键序列,与纤连蛋白作用的发挥密切相关。通常将其制成 c (RGDfK)、c (RGDyK) 等环肽,以增强稳定性。近年来研究发现,有 11 种整合素可与 RGD 肽特异性结合,为整合素的受体拮抗多肽。基于此,以 RGD 肽独特的靶向作用作为肿瘤治疗的新靶点,已成为肿瘤治疗研究的一大热点。同时,RGD 肽在血栓防治、骨组织诱导再生、抑制细胞粘附等领域也具有重要研究价值。
然而,RGD 环肽并非单一类型,根据成环原理的不同,可分为以下两类:
-
通过二硫键成环的含 RGD 序列环肽Cys 侧链的巯基可氧化形成 S-S 键,利用这一特性可将含 RGD 序列的多肽环化,得到 RGD 环肽。这类多肽的通式为 X1c (CRGDC) X2,其中 X1、X2 分别代表一段序列,序列中的 RGD 通过两端的两个 C 形成 S-S 键实现成环。其合成思路与常规 S-S 键氧化肽一致,均先采用固相法合成线性肽,再在液相中通过空气氧化法或碘氧化法形成 S-S 键环肽。
-
通过酰胺键成环的含 RGD 序列环肽最典型的 cyclo (Arg-Ala-Asp-d-Phe-Lys) 即通过酰胺键成环制备,通常在 G 与 D 之间通过酰胺键实现环化。线性肽先通过固相合成法合成,随后在液相环境中完成环化。该方法利用 N 端氨基酸的 α- 氨基与 C 端氨基酸的 α- 羧基发生酰胺缩合反应,形成酰胺键以实现成环。除这种 “头尾” 氨基与羧基成环的方式外,还包括两种成环形式:(1)侧链与侧链成环,即侧链氨基(如 Lys、Orn 侧链)与侧链羧基(如 Asp、Glu 侧链)成环;(2)侧链羧基(如 Asp、Glu 侧链)与 N 端氨基酸的 α- 氨基缩合成环。常见的 cyclo (Arg-Ala-Asp-d-Phe-Lys) 除基础环肽形式外,因其序列中 Lys 侧链带有活性氨基,可通过修饰 Lys 侧链氨基,得到多种修饰型 cyclo (Arg-Ala-Asp-d-Phe-Lys)。例如,在 Lys 侧链接合 FTIC 等荧光基团、DOTA 基团,或连接一段肽序列(如 Cys- (Pro) 10- cyclo (RGDfK))。这些修饰方式为 RGD 环肽的研究提供了丰富的多样性选择。
